Brak produktów w koszyku.

Wszystko co musisz wiedzieć na temat zespołu jelita drażliwego
Dieta / By
Michalina Mróz
Męczą Cię nawracające bóle brzucha, wzdęcia i gazy jelitowe? A może doskwiera Ci przewlekła biegunka lub zaparcie? To może być zespół jelita drażliwego! Z poniższego artykułu dowiesz się m.in. czym jest owe schorzenie, jak się je diagnozuje, a także co może pomóc w leczeniu przykrych dolegliwości.
Zespół jelita drażliwego – definicja i epidemiologia
Zespół jelita drażliwego (Irritable Bowel Syndrome, IBS) należy do czynnościowych chorób jelit o charakterze przewlekłym. Charakteryzuje się nieprawidłowym rytmem wypróżnień i bólami brzucha przy jednoczesnym braku odchyleń stwierdzanych w badaniach biochemicznych, morfologicznych, endoskopowych i obrazowych. Częstotliwość zachorowań wynosi 10–20% osób w populacji ogólnej. Na IBS chorują częściej kobiety niż mężczyźni, a objawy rozwijają się najczęściej w 30.-40. roku życia. Jednakże, niezależnie od wskazanego przedziału wiekowego, mogą one dotyczyć każdego wieku.
Etiopatogeneza
IBS stanowi najczęstsze schorzenie gastroenterologiczne, z którym spotykają się lekarze Podstawowej Opieki Zdrowotnej. Przyczyna jest prawdopodobnie złożona i nie do końca wyjaśniona. Wśród czynników mogących brać udział w patogenezie IBS wyróżnia się: czynniki genetyczne i psychospołeczne (zwłaszcza przewlekły stres o znacznym nasileniu), dysbiozę jelitową (obniżona ilość bakterii z rodzaju Lactobacillus i Bifidobacterium, zaś zwiększona ilość Escherichia coli, Streptoccocus, Clostridium spp. oraz zmiana proporcji między Bacteroidetes a Firmicutes). Niebagatelną rolę w powstawaniu IBS stanowią: nadwrażliwość trzewna, nieprawidłowa motoryka przewodu pokarmowego, zaburzenia immunologiczne w jelicie oraz ośrodkowym układzie nerwowym. Oś mózgowo-jelitowa jest pobudzana przez różne bodźce, które oddziałują na układ nerwowy lub przewód pokarmowy. Z jednej strony, stres psychiczny w IBS może negatywnie wpływać na układ pokarmowy, a z drugiej nasz nastrój mogą zmieniać również bodźce trzewne z jelit, zachowanie oraz odpowiedź ośrodkowego układu nerwowego na ból. W dotychczasowej literaturze naukowej nie udowodniono znaczenia nadwrażliwości na gluten i alergii pokarmowej w patogenezie IBS. Szacuje się, że u 8–31% osób, które w przeszłości przebyły infekcje przewodu pokarmowego, może wystąpić poinfekcyjny IBS o postaci biegunkowej.
Rozpoznanie
Diagnostyka IBS nie zawsze jest łatwa i często przysparza lekarzom nie lada problemów. Podstawę rozpoznania tego schorzenia stanowią Kryteria Rzymskie IV. Według nich, aby stwierdzić IBS niezbędne jest występowanie nawracającego bólu brzucha co najmniej 1 raz w tygodniu w okresie ostatnich 3 miesięcy. Początek objawów dotyczy minimum 6 miesięcy przed rozpoznaniem oraz wystąpienia co najmniej 2 z 3 poniższych kryteriów:
- związane jest z wypróżnieniem;
- ma związek ze zmianą częstotliwości wypróżnień;
- wiąże się ze zmianą konsystencji (wyglądu) stolca
W przypadku IBS bóle brzucha są niecharakterystyczne, o różnej i zmiennej lokalizacji, aczkolwiek najczęściej umiejscowione w podbrzuszu. Pacjenci z IBS skarżą się również na nawracające wzdęcia, uczucie parcia na stolec, zmianę liczby wypróżnień, nieprawidłowe uformowanie i/lub obecność śluzu w stolcu, co może ułatwić rozpoznanie tego schorzenia. Chorzy sugerują, że spożywanie posiłków nasila dolegliwości. Mogą pojawiać się także objawy spoza przewodu pokarmowego, jak np.: przewlekłe zmęczenie, bóle głowy, mięśni, zaburzenia snu, seksualne, psychiczne (lękowo-depresyjne) oraz w oddawaniu moczu. Ponadto u znacznej części pacjentów z IBS nakładają się objawy dyspepsji czynnościowej, refluksu żołądkowo-przełykowego oraz zespołu rozrostu bakteryjnego (small intestinal bacterial overgrowth, SIBO).
Na dzień dzisiejszy nie istnieją testy diagnostyczne potwierdzające IBS. Rozpoznanie stwierdza się na podstawie objawów zgłaszanych przez pacjenta. Poniżej przedstawiono tzw. „objawy alarmujące” (nie występujące w przypadku IBS) oraz najczęstsze choroby wymagające diagnostyki różnicowej.
Tab. 1. Objawy alarmujące oraz najważniejsze choroby wymagające różnicowania z IBS
Objawy alarmujące | Różnicowanie |
|
|
Postacie IBS
W zależności od rytmu wypróżnień i dominującej konsystencji stolca wyróżnia się następujące podtypy IBS: postać zaparciową, biegunkową, mieszaną lub niesklasyfikowaną. Podział ten został dokonany na podstawie Bristolskiej Skali Uformowania Stolca (BSUS).
Tab.2. Bristolska Skala Uformowania Stolca (BSUS)
Typ | Opis stolca |
1. | Pojedyncze zbite grudki podobne do orzechów, trudne do wydalenia |
2. | Stolec o wydłużonym kształcie, grudkowaty |
| 3. | Stolec wydłużony, z pęknięciami na powierzchni |
4. | Smukłe, wężowate kawałki stolca, gładkie miękkie |
| 5. | Miękkie drobiny z wyraźnymi krawędziami (łatwo wydalane) |
6. | Kłaczaste kawałki z postrzępionymi krawędziami |
7. | Wodnisty, bez stałych elementów (ciecz) |
Tab.3. Kryteria podziału zespołu jelita drażliwego na podtypy na podstawie BSUS
IBS-C | >25% wypróżnień ma uformowanie typu 1 i 2 oraz jednocześnie <25% wypróżnień ma uformowanie typu 6 i 7 |
IBS-D | >25% wypróżnień ma uformowanie typu 6 i 7 oraz jednocześnie <25% wypróżnień ma uformowanie typu 1 i 2 |
IBS-M | >25% wypróżnień ma uformowanie typu 1 i 2 oraz jednocześnie >25% wypróżnień ma uformowanie typu 6 i 7 |
IBS-U | <25% wypróżnień ma uformowanie typu 1 i 2 oraz typu 6 i 7 |
| |
Leczenie
IBS jest najczęstszą, przewlekłą, czynnościową chorobą jelit. Mimo że ma znaczący wpływ na jakość życia pacjenta, nie należy do chorób śmiertelnych. Z uwagi na fakt, że jednoznaczna przyczyna IBS nie jest znana, niestety nie ma możliwości trwałego wyleczenia, a objawy często nawracają. Aczkolwiek warto podkreślić łagodny charakter schorzenia i pomyślne rokowanie. Celem leczenia pacjentów z IBS powinno być dążenie do zredukowania uciążliwych objawów towarzyszących chorobie oraz poprawa jakości życia chorego. Wobec czego, kluczowym elementem postępowania terapeutycznego jest prawidłowa diagnoza oraz utrzymywanie dobrej relacji pomiędzy lekarzem a pacjentem, dzięki czemu istnieje możliwość budowania wzajemnego zaufania i poczucia bezpieczeństwa.
Istotną kwestię w leczeniu IBS stanowi zmiana stylu życia (regularna aktywność fizyczna, dbanie o dobry sen, eliminacja używek i umiejętność zarządzania stresem) oraz modyfikacje żywieniowe (unikanie spożywania produktów nasilających dolegliwości). W postaci zaparciowej IBS podkreśla się rolę rozpuszczalnej frakcji błonnika pokarmowego (babka płesznik, babka jajowata) w łagodzeniu objawów.
W ostatnim czasie obserwuje się zwiększone zainteresowanie dietą ubogą w fermentujące oligo-, di-, monosacharydy i poliole (Fermentable Oligo-, Di- and Monosaccharides and Polyols, FODMAPs). Do grup produktów bogatych w FODMAPs należą m.in.: pszenica, laktoza, nasiona roślin strączkowych, warzywa takie jak: czosnek, cebula, kapusta, brokuł, niektóre owoce, np. jabłka, gruszki, śliwki oraz słodziki z końcówką „-ol” (ksylitol, sorbitol, maltitol, mannitol). Z uwagi na wysoki stopień fermentacji, zaś słabą wchłanialność, FODMAPs mogą indukować dolegliwości żołądkowo-jelitowe u pacjentów z IBS. Liczne badania naukowe potwierdzają skuteczność diety z ograniczeniem FODMAPs w łagodzeniu objawów ze strony przewodu pokarmowego u osób chorujących na IBS. Jednakże ze względu na dosyć restrykcyjny charakter diety i ryzyko niedoborów żywieniowych powinna być stosowana krótkoterminowo oraz pod okiem wykwalifikowanego dietetyka. Rekomendowana jest spersonalizowana dieta z określeniem indywidualnego progu tolerancji na produkty o wysokiej zawartości FODMAPs. W przypadku stwierdzonej nietolerancji laktozy zasadne jest ograniczenie do minimum lub wykluczenie z diety tego składnika. Natomiast stosowanie diety bezglutenowej nie ma uzasadnienia w IBS.
W łagodzeniu dolegliwości ze strony przewodu pokarmowego pomocne mogą okazać się probiotyki, czyli żywe drobnoustroje, które podawane w odpowiednich ilościach, wywołują korzystny efekt zdrowotny. Obiecujące dane naukowe dotyczą szczepu Lactobacillus plantarum DSM 9843 (299v) w przypadku dorosłych, natomiast u dzieci – szczep Lactobacillus GG oraz poliprobiotyk VSL#3. W zależności od dominujących objawów niekiedy wymagane jest stosowanie leków rozkurczowych, przeciwbiegunkowych lub przeciwzaparciowych. Jeśli nie zaobserwujemy poprawy po zastosowaniu wyżej omówionych metod leczenia, koniecznie może okazać się użycie trójpierścieniowych leków przeciwdepresyjnych lub selektywnych inhibitorów wychwytu zwrotnego serotoniny.
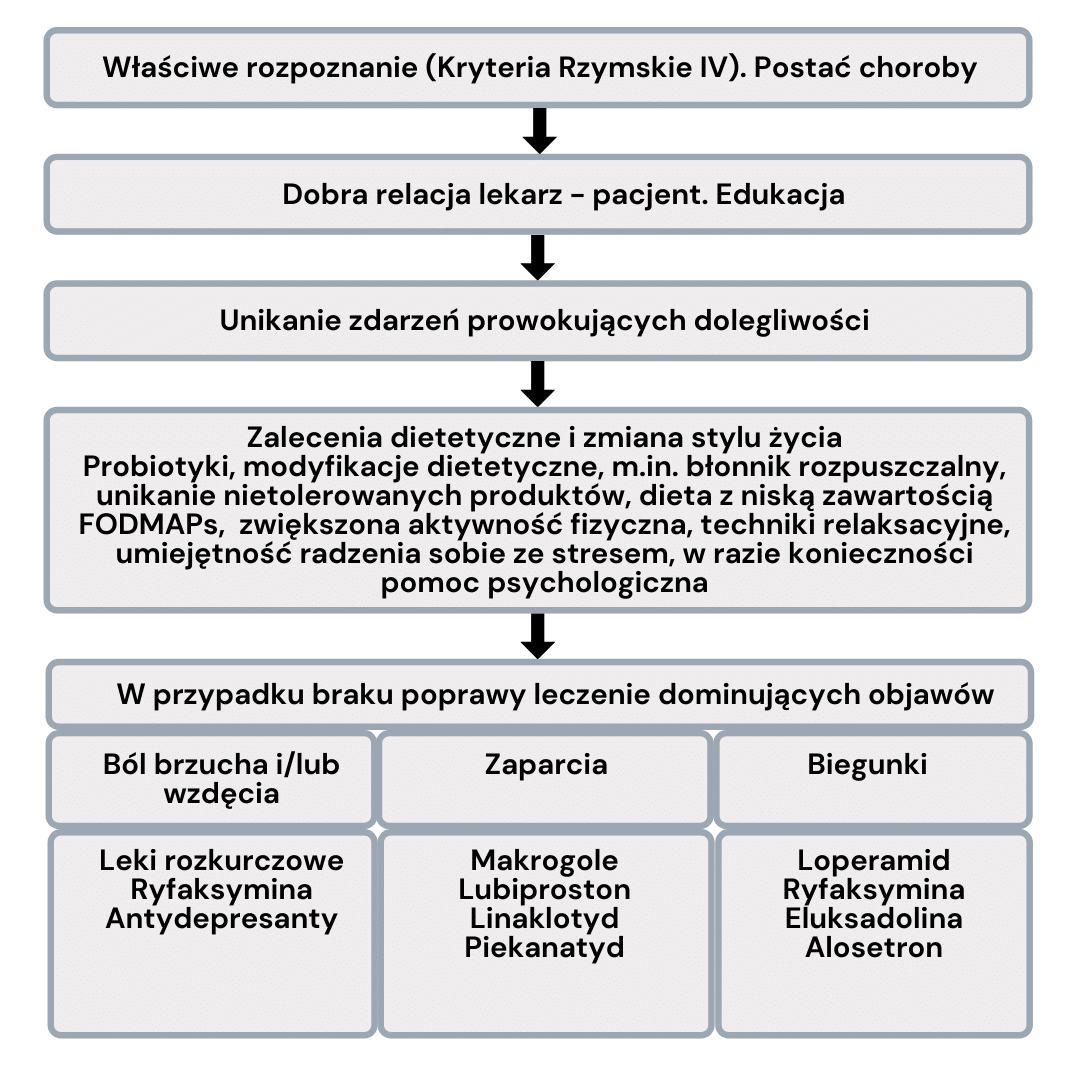
Na poniższej grafice przedstawiono schemat postępowania w przypadku podejrzenia IBS.
Strategia diagnostyczno-lecznicza w IBS na podstawie publikacji Adrych K. Zespół jelita drażliwego w świetle najnowszych wytycznych. Forum Medycyny Rodzinnej 2018; 12(6): 224-233
Podsumowanie
- IBS to częsta i nawracająca choroba, która, pomimo dosyć łagodnego charakteru i dobrego rokowania, znacząco pogarsza jakość życia osób zmagających się z tym schorzeniem.
- Patogeneza tej choroby jest złożona i nie do końca poznana.
- IBS stanowi najczęstszą, przewlekłą, czynnościową chorobą jelit, która charakteryzuje się bólem brzucha związanym ze zmianą częstości oddawania stolca i/lub jego wyglądu.
- Aktualne rozpoznanie należy stawiać opierając się na Kryteriach Rzymskich IV, ograniczając przy tym do minimum badania dodatkowe.
- Leczenie IBS obejmuje: dobrą relację lekarz-pacjent, modyfikacje stylu życia, farmako- i/lub psychoterapię.
- Adrych K. Zespół jelita drażliwego w świetle najnowszych wytycznych. Forum Medycyny Rodzinnej 2018; 12(6): 224-233.
- Catassi G, Lionetti E, Gatti S, et al. The low FODMAP diet. Many question marks for a catchy acronym. Nutrients 2017; 9: 292.
- Kennedy T, Jones R, Hungin A, et al. Irritable bowel syndrome, gastro-oesophageal reflux, and bronchial hyper-responsiveness in the general population. Gut 1998; 43(6): 770–774.
- Lacy BE, Mearin F, Chang L, et al. Bowel disorders. Gastroenterology 2016; 150: 1393–1407.
- Lovell RM, Ford AC: Global prevalence of and risk factors for irritable bowel syndrome: ameta-analysis. Clin Gastroenterol Hepatol 2012; 7: 712–721.
- Lewis SJ, Heaton KW: Stool form scale as a useful guide to intestinal transit time. Sand J Gastroenterol 1997; 32(9): 920–924.
- Schumann D, Klose P, Lauche R, et al: Low fermentable, oligo-, di-, monosaccharides and polyol diet in the treatment of irritable bowel syndrome: a systematic review and meta-analysis. Nutrition 2018; 45: 24–31.
- Szajewska H: Probiotyki – aktualny stan wiedzy i zalecenia dla praktyki klinicznej. Med. Prakt. 2017; 7-8: 19–37.
- Tunitsky M, Gardner G: Węglowodany FODMAP i Ty. In: STOP zespołowi jelita drażliwego. Dieta FODMAP. 1st ed., Rebis, Poznań 2018: 4–39.
